

普米斯多款创新药研究成果对外公布@AACR 2022@SITC 2021
- 分类:新闻动态
- 作者:
- 来源:
- 发布时间:2022-04-15
- 访问量:0
【概要描述】 普米斯生物技术公司(以下简称“普米斯”)在2022年第113届美国癌症研究协会年会(AACR 2022)公布了其自主研发的6款抗体新药的研究成果,包括4款多特异性抗体:PM1022(PD-L1/TIGIT)、PM1009(TIGIT/PVRIG)、PM4008(CEACAM5&6/CD3)、PM1032(CLDN18.2/4-1BB),以及2款单克隆抗体:PM1038(CD39)、PM1015(CD73)。此外,普米斯在2021年第36届癌症免疫治疗学会年会(SITC 2021)公布了其自主研发的双特异性抗体PM1003(PD-L1/4-1BB)的研究成果。以上项目研究成果公布如下:
双特异性抗体PM1022(PD-L1/TIGIT)
PM1022是抗PD-L1/TIGIT双特异性抗体。临床前研究显示,PM1022可高亲和力结合人和恒河猴的PD-L1和TIGIT,同时高效阻断PD-1/PD-L1以及TIGIT/CD155/CD112免疫抑制信号通路。在小鼠模型中,PM1022可剂量依赖性地抑制肿瘤生长,且抗肿瘤活性显著优于Keytruda治疗组。提示,PM1022是极具临床开发价值的分子,现已获国家药品监督管理局(NMPA)批准开展I期临床研究。
双特异性抗体PM1009(TIGIT/PVRIG)
PM1009是抗TIGIT/PVRIG双特异性抗体。临床前研究显示,PM1009可高亲和力结合人和食蟹猴的TIGIT 和PVRIG,同时解除TIGIT/CD155/CD112以及PVRIG/CD112免疫抑制信号,并顺式增强CD226激活信号。在PD-1单抗耐药模型中,PM1009与抗PD-1单抗联用,具有显著优于TIGIT单抗或PVRIG单抗联合PD-1单抗的抗肿瘤活性。
单克隆抗体PM1038(CD39)
CD39-CD73-腺苷通路是Treg细胞发挥免疫抑制功能的重要途径,在部分自身免疫性疾病、肿瘤、人免疫缺陷病毒感染中发现Treg细胞等免疫抑制性细胞以及某些肿瘤细胞中CD39、CD73表达水平异常升高。与大多数在研抗CD39单抗不同,PM1038是识别CD39双表位的单域抗体,能够完全阻断膜型和可溶性CD39的酶活活性,且优于对照抗体。在体内药效模型中,PM1038显示出一定的单药抗肿瘤活性,与抗CD73单抗联用时抗肿瘤活性更强。基于PM1038构建的抗PD-1/CD39双特异性抗体在体内移植瘤模型中表现出明显优于PD-1单抗抗肿瘤作用。
多特异性抗体PM4008(CEACAM5&6/CD3)
普米斯自主研发了差异化设计的 T cell engager平台(M-body),优化了CD3端的结合活性并去除了与FcγR的结合,大大降低了非抗原依赖性激活,在减轻了系统性T细胞过度激活导致的毒性的同时增强了抗肿瘤活性。PM4008可通过同时结合肿瘤细胞表面抗原CEACAM5/6和T细胞表面抗原CD3形成免疫突触,激活 T细胞和促进T细胞增殖,进而特异性杀伤肿瘤细胞。
双特异性抗体PM1032(CLDN18.2/4-1BB)
PM1032是一种条件激活型4-1BB激动剂,能够在高表达CLDN18.2的肿瘤局部诱导CLDN18.2依赖的特异性4-1BB信号通路的激活,增强肿瘤微环境中的T细胞活性并诱导肿瘤抗原特异性的记忆T细胞的生成。同时,独特的4-1BB结合位点以及对Fc的改造最大限度地降低了PM1032在CLDN18.2阴性环境中对T细胞的激活,大大降低了系统性毒性。在体内药效研究中,PM1032可使多种肿瘤移植瘤消退,并且伴随着免疫记忆的产生,治愈后的小鼠再次接种同种肿瘤细胞后不能成瘤。在恒河猴重复给药毒性试验中,以最高给药剂量150 mg/kg给药的安全性和耐受性良好。PM1032现已获NMPA批准开展I期临床研究。
单克隆抗体PM1015(CD73)
CD73在肿瘤免疫微环境(TME)中主要通过介导腺苷的产生而发挥抑制性免疫调节作用。与大多数在研抗CD73单抗不同,PM1015能结合独特的抗原表位,可在多种表达CD73的肿瘤细胞系中完全阻断膜型CD73的酶活活性。此外,PM1015还可完全阻断可溶性CD73的酶活活性,未见“钩状效应”(hook effect)。体内药效试验表明,PM1015可有效抑制多种小鼠肿瘤模型的生长,并显示出良好的剂量依赖性抗肿瘤活性;PM1015与抗PD-1单抗(PM1028)联用可显著增强抗肿瘤作用,抑瘤作用优于二者单独给药。在恒河猴和大鼠重复给药毒性试验中,以最高给药剂量 500 mg/kg给药的安全性和耐受性良好。PM1015现已获NMPA批准开展I期临床研究。
双特异性抗体PM1003(PD-L1/4-1BB)
PM1003是抗PD-L1/4-1BB双特异性抗体,其中抗4-1BB端是目前公开报道的唯一仅结合4-1BB蛋白CRD4的分子,其独特的结合位点为平衡4-1BB激动剂的安全性和有效性提供了可能;PM1003分子在高效阻断PD-L1/PD-1免疫抑制信号的同时,具有PD-L1交联依赖的4-1BB信号激活活性,在多种小鼠模型中能够显著抑制肿瘤生长,且可以诱导长期肿瘤免疫记忆效应。与同类产品相比,PM1003对转基因小鼠的肝脏毒性明显降低;在NHP重复给药毒性试验中,在最高剂量为150 mg/kg下安全性和耐受性良好,抗药抗体产生率较低。提示,PM1003是兼具安全性和有效性的新一代免疫治疗分子,目前正在开展I期临床研究。
关于普米斯
普米斯于2018年注册成立,一直秉承“点亮创新火种,成就健康人生”的创业使命,聚焦恶性肿瘤及自身免疫疾病,致力于国家1类创新生物药的研发及产业化。核心团队具有务实的国内外创新生物药研发、药政策略、产业化和商业化经验,正在推进超过20个1类生物新药项目,现有多个新药项目处于临床研究阶段。普米斯在珠海、苏州和香港均设有新药研发中心,在上海、北京设立临床研究中心,并在南通建设产业化生产基地,未来普米斯将凭借其高价值的产品链、强大的创新能力、经验丰富的核心团队迅速跻身国内生物制药企业第一梯队。
普米斯多款创新药研究成果对外公布@AACR 2022@SITC 2021
【概要描述】 普米斯生物技术公司(以下简称“普米斯”)在2022年第113届美国癌症研究协会年会(AACR 2022)公布了其自主研发的6款抗体新药的研究成果,包括4款多特异性抗体:PM1022(PD-L1/TIGIT)、PM1009(TIGIT/PVRIG)、PM4008(CEACAM5&6/CD3)、PM1032(CLDN18.2/4-1BB),以及2款单克隆抗体:PM1038(CD39)、PM1015(CD73)。此外,普米斯在2021年第36届癌症免疫治疗学会年会(SITC 2021)公布了其自主研发的双特异性抗体PM1003(PD-L1/4-1BB)的研究成果。以上项目研究成果公布如下:
双特异性抗体PM1022(PD-L1/TIGIT)
PM1022是抗PD-L1/TIGIT双特异性抗体。临床前研究显示,PM1022可高亲和力结合人和恒河猴的PD-L1和TIGIT,同时高效阻断PD-1/PD-L1以及TIGIT/CD155/CD112免疫抑制信号通路。在小鼠模型中,PM1022可剂量依赖性地抑制肿瘤生长,且抗肿瘤活性显著优于Keytruda治疗组。提示,PM1022是极具临床开发价值的分子,现已获国家药品监督管理局(NMPA)批准开展I期临床研究。
双特异性抗体PM1009(TIGIT/PVRIG)
PM1009是抗TIGIT/PVRIG双特异性抗体。临床前研究显示,PM1009可高亲和力结合人和食蟹猴的TIGIT 和PVRIG,同时解除TIGIT/CD155/CD112以及PVRIG/CD112免疫抑制信号,并顺式增强CD226激活信号。在PD-1单抗耐药模型中,PM1009与抗PD-1单抗联用,具有显著优于TIGIT单抗或PVRIG单抗联合PD-1单抗的抗肿瘤活性。
单克隆抗体PM1038(CD39)
CD39-CD73-腺苷通路是Treg细胞发挥免疫抑制功能的重要途径,在部分自身免疫性疾病、肿瘤、人免疫缺陷病毒感染中发现Treg细胞等免疫抑制性细胞以及某些肿瘤细胞中CD39、CD73表达水平异常升高。与大多数在研抗CD39单抗不同,PM1038是识别CD39双表位的单域抗体,能够完全阻断膜型和可溶性CD39的酶活活性,且优于对照抗体。在体内药效模型中,PM1038显示出一定的单药抗肿瘤活性,与抗CD73单抗联用时抗肿瘤活性更强。基于PM1038构建的抗PD-1/CD39双特异性抗体在体内移植瘤模型中表现出明显优于PD-1单抗抗肿瘤作用。
多特异性抗体PM4008(CEACAM5&6/CD3)
普米斯自主研发了差异化设计的 T cell engager平台(M-body),优化了CD3端的结合活性并去除了与FcγR的结合,大大降低了非抗原依赖性激活,在减轻了系统性T细胞过度激活导致的毒性的同时增强了抗肿瘤活性。PM4008可通过同时结合肿瘤细胞表面抗原CEACAM5/6和T细胞表面抗原CD3形成免疫突触,激活 T细胞和促进T细胞增殖,进而特异性杀伤肿瘤细胞。
双特异性抗体PM1032(CLDN18.2/4-1BB)
PM1032是一种条件激活型4-1BB激动剂,能够在高表达CLDN18.2的肿瘤局部诱导CLDN18.2依赖的特异性4-1BB信号通路的激活,增强肿瘤微环境中的T细胞活性并诱导肿瘤抗原特异性的记忆T细胞的生成。同时,独特的4-1BB结合位点以及对Fc的改造最大限度地降低了PM1032在CLDN18.2阴性环境中对T细胞的激活,大大降低了系统性毒性。在体内药效研究中,PM1032可使多种肿瘤移植瘤消退,并且伴随着免疫记忆的产生,治愈后的小鼠再次接种同种肿瘤细胞后不能成瘤。在恒河猴重复给药毒性试验中,以最高给药剂量150 mg/kg给药的安全性和耐受性良好。PM1032现已获NMPA批准开展I期临床研究。
单克隆抗体PM1015(CD73)
CD73在肿瘤免疫微环境(TME)中主要通过介导腺苷的产生而发挥抑制性免疫调节作用。与大多数在研抗CD73单抗不同,PM1015能结合独特的抗原表位,可在多种表达CD73的肿瘤细胞系中完全阻断膜型CD73的酶活活性。此外,PM1015还可完全阻断可溶性CD73的酶活活性,未见“钩状效应”(hook effect)。体内药效试验表明,PM1015可有效抑制多种小鼠肿瘤模型的生长,并显示出良好的剂量依赖性抗肿瘤活性;PM1015与抗PD-1单抗(PM1028)联用可显著增强抗肿瘤作用,抑瘤作用优于二者单独给药。在恒河猴和大鼠重复给药毒性试验中,以最高给药剂量 500 mg/kg给药的安全性和耐受性良好。PM1015现已获NMPA批准开展I期临床研究。
双特异性抗体PM1003(PD-L1/4-1BB)
PM1003是抗PD-L1/4-1BB双特异性抗体,其中抗4-1BB端是目前公开报道的唯一仅结合4-1BB蛋白CRD4的分子,其独特的结合位点为平衡4-1BB激动剂的安全性和有效性提供了可能;PM1003分子在高效阻断PD-L1/PD-1免疫抑制信号的同时,具有PD-L1交联依赖的4-1BB信号激活活性,在多种小鼠模型中能够显著抑制肿瘤生长,且可以诱导长期肿瘤免疫记忆效应。与同类产品相比,PM1003对转基因小鼠的肝脏毒性明显降低;在NHP重复给药毒性试验中,在最高剂量为150 mg/kg下安全性和耐受性良好,抗药抗体产生率较低。提示,PM1003是兼具安全性和有效性的新一代免疫治疗分子,目前正在开展I期临床研究。
关于普米斯
普米斯于2018年注册成立,一直秉承“点亮创新火种,成就健康人生”的创业使命,聚焦恶性肿瘤及自身免疫疾病,致力于国家1类创新生物药的研发及产业化。核心团队具有务实的国内外创新生物药研发、药政策略、产业化和商业化经验,正在推进超过20个1类生物新药项目,现有多个新药项目处于临床研究阶段。普米斯在珠海、苏州和香港均设有新药研发中心,在上海、北京设立临床研究中心,并在南通建设产业化生产基地,未来普米斯将凭借其高价值的产品链、强大的创新能力、经验丰富的核心团队迅速跻身国内生物制药企业第一梯队。
- 分类:新闻动态
- 作者:
- 来源:
- 发布时间:2022-04-15
- 访问量:0
普米斯生物技术公司(以下简称“普米斯”)在2022年第113届美国癌症研究协会年会(AACR 2022)公布了其自主研发的6款抗体新药的研究成果,包括4款多特异性抗体:PM1022(PD-L1/TIGIT)、PM1009(TIGIT/PVRIG)、PM4008(CEACAM5&6/CD3)、PM1032(CLDN18.2/4-1BB),以及2款单克隆抗体:PM1038(CD39)、PM1015(CD73)。此外,普米斯在2021年第36届癌症免疫治疗学会年会(SITC 2021)公布了其自主研发的双特异性抗体PM1003(PD-L1/4-1BB)的研究成果。以上项目研究成果公布如下:
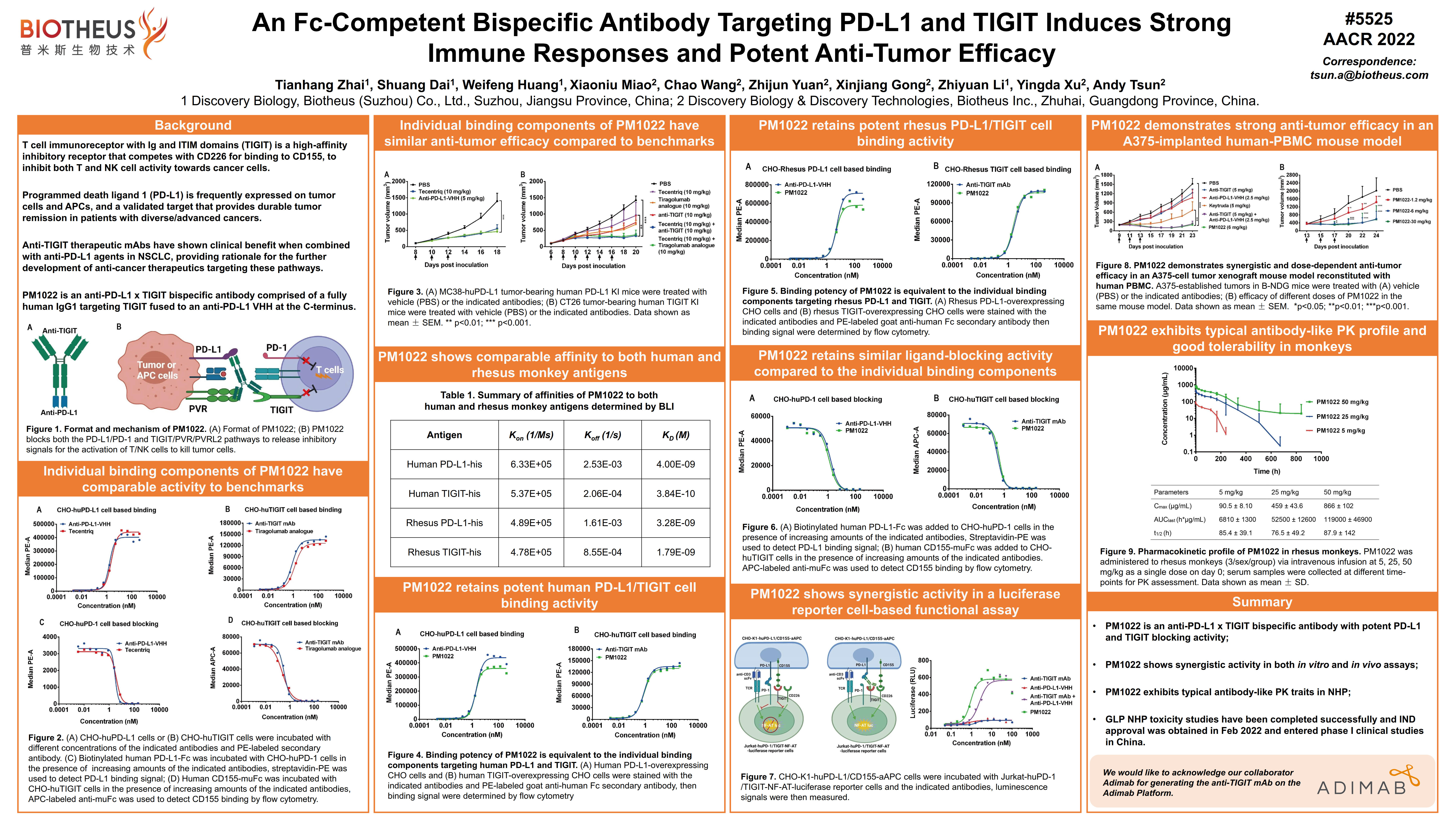
双特异性抗体PM1022(PD-L1/TIGIT)
PM1022是抗PD-L1/TIGIT双特异性抗体。临床前研究显示,PM1022可高亲和力结合人和恒河猴的PD-L1和TIGIT,同时高效阻断PD-1/PD-L1以及TIGIT/CD155/CD112免疫抑制信号通路。在小鼠模型中,PM1022可剂量依赖性地抑制肿瘤生长,且抗肿瘤活性显著优于Keytruda治疗组。提示,PM1022是极具临床开发价值的分子,现已获国家药品监督管理局(NMPA)批准开展I期临床研究。
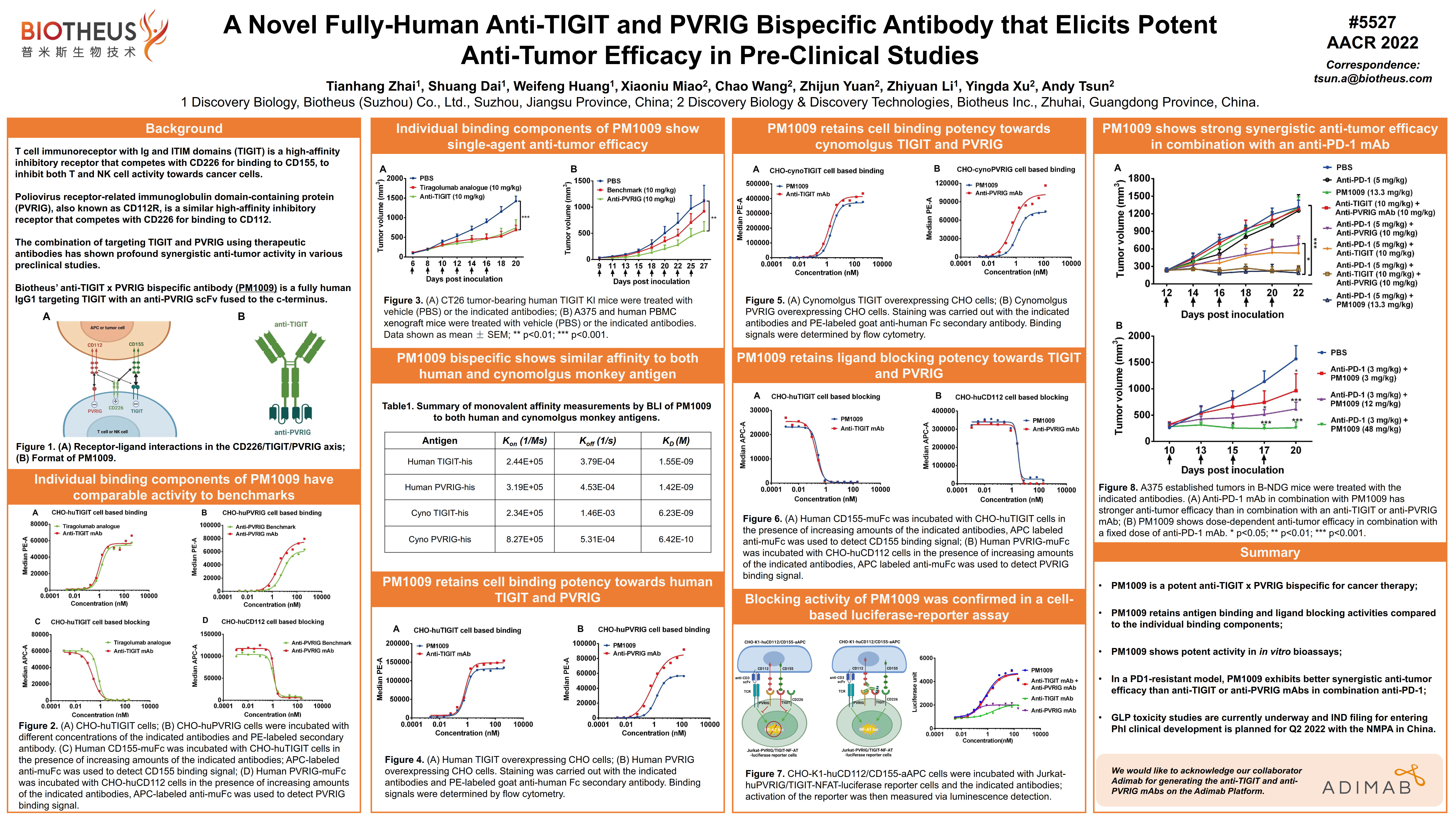
双特异性抗体PM1009(TIGIT/PVRIG)
PM1009是抗TIGIT/PVRIG双特异性抗体。临床前研究显示,PM1009可高亲和力结合人和食蟹猴的TIGIT 和PVRIG,同时解除TIGIT/CD155/CD112以及PVRIG/CD112免疫抑制信号,并顺式增强CD226激活信号。在PD-1单抗耐药模型中,PM1009与抗PD-1单抗联用,具有显著优于TIGIT单抗或PVRIG单抗联合PD-1单抗的抗肿瘤活性。
单克隆抗体PM1038(CD39)
CD39-CD73-腺苷通路是Treg细胞发挥免疫抑制功能的重要途径,在部分自身免疫性疾病、肿瘤、人免疫缺陷病毒感染中发现Treg细胞等免疫抑制性细胞以及某些肿瘤细胞中CD39、CD73表达水平异常升高。与大多数在研抗CD39单抗不同,PM1038是识别CD39双表位的单域抗体,能够完全阻断膜型和可溶性CD39的酶活活性,且优于对照抗体。在体内药效模型中,PM1038显示出一定的单药抗肿瘤活性,与抗CD73单抗联用时抗肿瘤活性更强。基于PM1038构建的抗PD-1/CD39双特异性抗体在体内移植瘤模型中表现出明显优于PD-1单抗抗肿瘤作用。

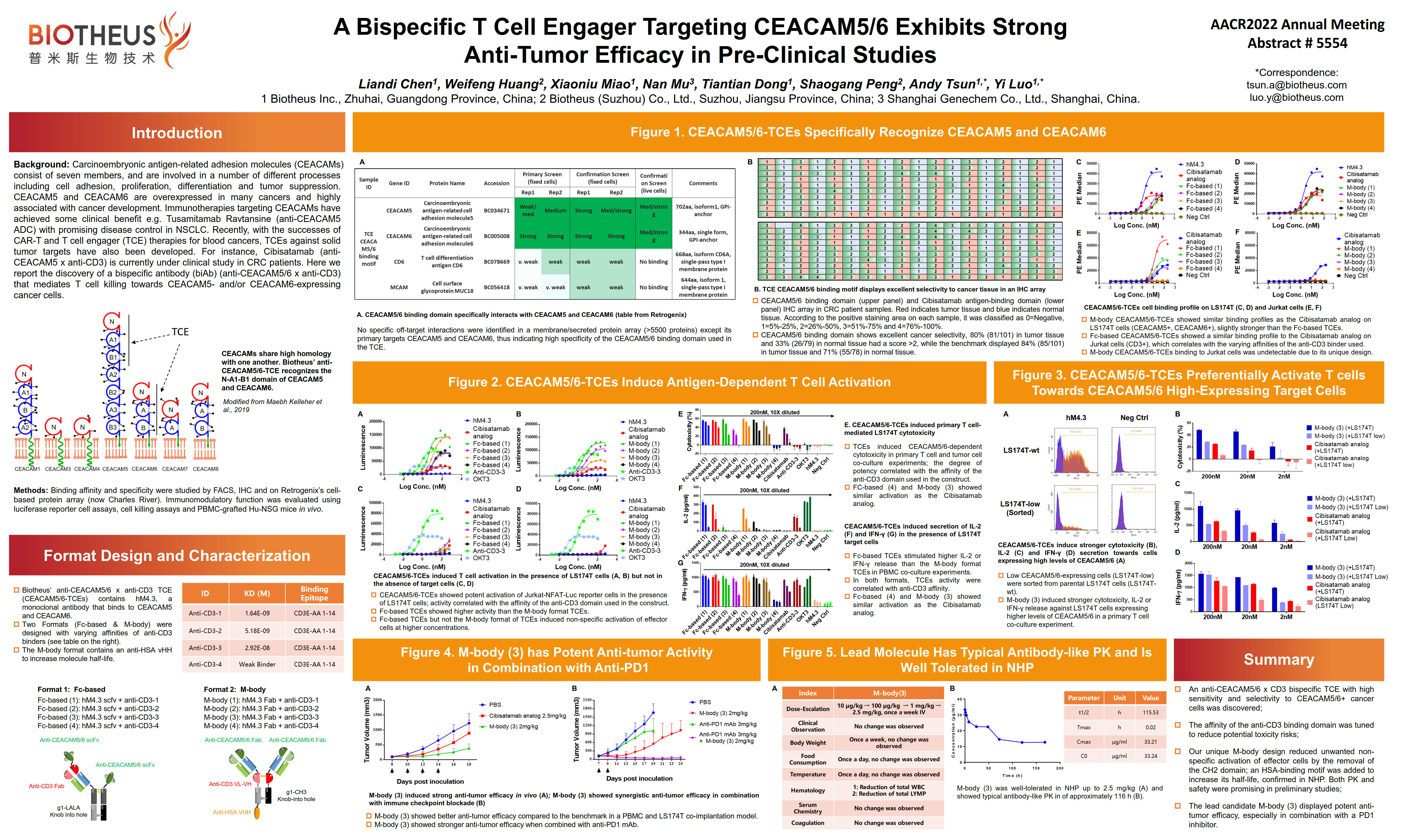
多特异性抗体PM4008(CEACAM5&6/CD3)
普米斯自主研发了差异化设计的 T cell engager平台(M-body),优化了CD3端的结合活性并去除了与FcγR的结合,大大降低了非抗原依赖性激活,在减轻了系统性T细胞过度激活导致的毒性的同时增强了抗肿瘤活性。PM4008可通过同时结合肿瘤细胞表面抗原CEACAM5/6和T细胞表面抗原CD3形成免疫突触,激活 T细胞和促进T细胞增殖,进而特异性杀伤肿瘤细胞。
双特异性抗体PM1032(CLDN18.2/4-1BB)
PM1032是一种条件激活型4-1BB激动剂,能够在高表达CLDN18.2的肿瘤局部诱导CLDN18.2依赖的特异性4-1BB信号通路的激活,增强肿瘤微环境中的T细胞活性并诱导肿瘤抗原特异性的记忆T细胞的生成。同时,独特的4-1BB结合位点以及对Fc的改造最大限度地降低了PM1032在CLDN18.2阴性环境中对T细胞的激活,大大降低了系统性毒性。在体内药效研究中,PM1032可使多种肿瘤移植瘤消退,并且伴随着免疫记忆的产生,治愈后的小鼠再次接种同种肿瘤细胞后不能成瘤。在恒河猴重复给药毒性试验中,以最高给药剂量150 mg/kg给药的安全性和耐受性良好。PM1032现已获NMPA批准开展I期临床研究。

单克隆抗体PM1015(CD73)
CD73在肿瘤免疫微环境(TME)中主要通过介导腺苷的产生而发挥抑制性免疫调节作用。与大多数在研抗CD73单抗不同,PM1015能结合独特的抗原表位,可在多种表达CD73的肿瘤细胞系中完全阻断膜型CD73的酶活活性。此外,PM1015还可完全阻断可溶性CD73的酶活活性,未见“钩状效应”(hook effect)。体内药效试验表明,PM1015可有效抑制多种小鼠肿瘤模型的生长,并显示出良好的剂量依赖性抗肿瘤活性;PM1015与抗PD-1单抗(PM1028)联用可显著增强抗肿瘤作用,抑瘤作用优于二者单独给药。在恒河猴和大鼠重复给药毒性试验中,以最高给药剂量 500 mg/kg给药的安全性和耐受性良好。PM1015现已获NMPA批准开展I期临床研究。

双特异性抗体PM1003(PD-L1/4-1BB)
PM1003是抗PD-L1/4-1BB双特异性抗体,其中抗4-1BB端是目前公开报道的唯一仅结合4-1BB蛋白CRD4的分子,其独特的结合位点为平衡4-1BB激动剂的安全性和有效性提供了可能;PM1003分子在高效阻断PD-L1/PD-1免疫抑制信号的同时,具有PD-L1交联依赖的4-1BB信号激活活性,在多种小鼠模型中能够显著抑制肿瘤生长,且可以诱导长期肿瘤免疫记忆效应。与同类产品相比,PM1003对转基因小鼠的肝脏毒性明显降低;在NHP重复给药毒性试验中,在最高剂量为150 mg/kg下安全性和耐受性良好,抗药抗体产生率较低。提示,PM1003是兼具安全性和有效性的新一代免疫治疗分子,目前正在开展I期临床研究。

关于普米斯
普米斯于2018年注册成立,一直秉承“点亮创新火种,成就健康人生”的创业使命,聚焦恶性肿瘤及自身免疫疾病,致力于国家1类创新生物药的研发及产业化。核心团队具有务实的国内外创新生物药研发、药政策略、产业化和商业化经验,正在推进超过20个1类生物新药项目,现有多个新药项目处于临床研究阶段。普米斯在珠海、苏州和香港均设有新药研发中心,在上海、北京设立临床研究中心,并在南通建设产业化生产基地,未来普米斯将凭借其高价值的产品链、强大的创新能力、经验丰富的核心团队迅速跻身国内生物制药企业第一梯队。
扫二维码用手机看
推荐阅读
- 普米斯宣布与翰森制药就扩大开发EGFR/cMet双特异性抗体药物达成战略合作 2024.03.14
- 普米斯宣布PM8002(抗PD-L1/VEGF双抗)成功纳入“突破性治疗品种名单” 2024.03.09
- 普米斯宣布与Bitterroot Bio达成战略合作 2024.02.27
- SABCS 2023 | 普米斯公布双特异性抗体PM8002联合白蛋白紫杉醇一线治疗晚期三阴性乳腺癌的最新临床进展 2023.12.13
- 普米斯宣布与BioNTech(百欧恩泰)达成战略合作 2023.11.06
- SITC 2023│普米斯公布2款双特异性抗体最新研究成果 2023.11.04



